Digiuno intermittente e microbiota

Le festività natalizie si avvicinano e, si sa, le nostre tavole tendono a riempirsi di cibo più del solito.
Così noi abbiamo deciso di parlarvi di digiuno intermittente e della sua relazione con il microbiota intestinale.
Schemi di digiuno intermittente
Per digiuno intermittente si intende la pratica di alternare periodi di normale assunzione di cibo a periodi di digiuno, di durata variabile, in base allo schema dietetico seguito.
Un protocollo tipico di digiuno intermittente prevede un digiuno per 12 o 16 ore al giorno e il consumo dei pasti nelle ore restanti, eseguito in genere su un massimo di 2 giorni alla settimana.
Altri schemi prevedono, invece, apporti calorici imitanti il digiuno (circa 500-600 kcal) durante 2 giorni in una settimana, mentre i restanti 5 si mangia normalmente.
Una pratica alternativa, infine, prevede il digiuno per 24 ore consecutive, uno o due giorni alla settimana.
Relazione tra digiuno e microbiota
Recenti studi hanno dimostrato come il digiuno intermittente sia in grado di apportare diversi benefici alla salute, in termini di miglioramento dell’obesità, dell’insulino resistenza e dei livelli di colesterolo LDL.
Le esatte dinamiche rimangono ancora da definire, ma ci sono evidenze che suggeriscono un possibile ruolo del microbiota intestinale come mediatore di tali effetti sul metabolismo.
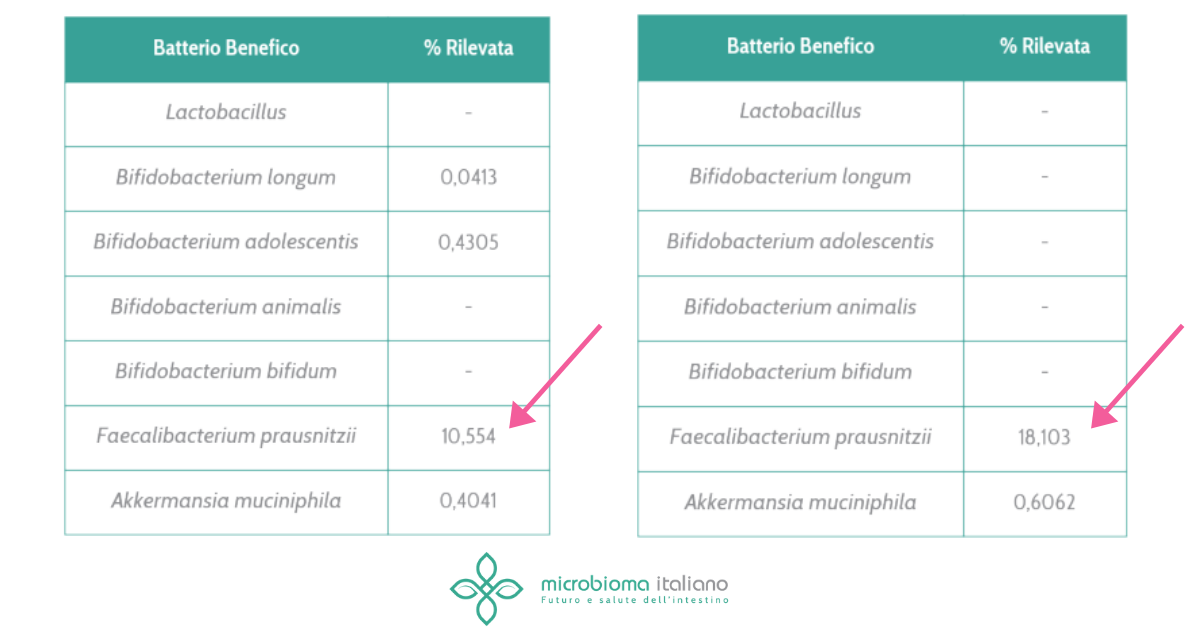
In particolare, è emerso che il digiuno intermittente è in grado di influenzare la composizione del microbiota intestinale, determinando l’aumento della specie Akkermansia muciniphila (nota per i suoi effetti benefici sul metabolismo dell’ospite) e la riduzione di Rikenellaceae, Ruminococcaceae e del genere Alistipes. A ciò si aggiunge un aumento dei livelli plasmatici di alcuni prodotti della fermentazione microbica, in particolare acetato e lattato.
L’ipotesi del browning
L’ipotesi avanzata è che tali alterazioni possano promuovere un fenomeno chiamato browning, in cui le cellule del tessuto adiposo bianco, deputate all’immagazzinamento energetico, sono “riprogrammate” per assumere caratteristiche simili alle cellule del tessuto adiposo bruno, coinvolte nella termoregolazione.
Queste ultime sono ricche in mitocondri e costituiscono una sorta di grasso “brucia grassi”, in quanto non immagazzinano energia, ma la disperdono sotto forma di calore.
Un’ulteriore evidenza emersa da questi studi è che la risposta del microbiota intestinale al digiuno varia in base alla durata e gli effetti maggiori sono stati osservati con un intervallo di 16 ore tra un pasto e l’altro.
Tuttavia, le alterazioni promosse dal digiuno sul microbiota sono transitorie, in quanto la ripresa della normale alimentazione ne induce la perdita.
Sono necessari, quindi, ulteriori studi al fine di comprendere meglio i meccanismi e potenziare i benefici di questa pratica a lungo termine.
Ricordiamo che la pratica del digiuno intermittente potrebbe non essere raccomandata per tutti i soggetti e che ogni intervento nutrizionale va sempre personalizzato, con la guida di un professionista.
Alla prossima!
Ilena Li Mura
Biologa Nutrizionista
Reference:
- Fasting the Microbiota to Improve Metabolism? Joel T. Haas and Bart Staels, 2017.
- Intermittent fasting and gut microbiota. Karakan T. 2019
- The effects of daily fasting hours on shaping gut microbiota in mice. Li et al, 2020.