Microbiota e Diabete

In vista della giornata mondiale del diabete, il 14 novembre 2020, noi di Microbioma Italiano abbiamo voluto fare un piccolo excursus sul forte legame tra microbiota intestinale e questa patologia sempre più comune. Un legame da cui è possibile trarre molti insegnamenti e benefici.
Il diabete è una patologia che può insorgere nei bambini e negli adolescenti per motivi genetici, virali o di stress (si parla allora di tipo 1). Tuttavia nel 90% dei casi può emergere anche in un soggetto adulto a causa di uno stile di vita sedentario, obesità, presenza di grasso viscerale, dieta povera di fibre e ricca in grassi saturi e zuccheri. La predisposizione genetica deve essere presente ma abitudini sbagliate sono il trigger principale del diabete di tipo 2.
Cosa vuol dire diabete?
Essere diabetici implica non essere in grado di gestire l’assunzione di zuccheri semplici o complessi. Questo accade perché l’insulina, l’ormone deputato alla gestione del metabolismo del glucosio, è carente oppure le cellule e i tessuti su cui agisce ne sono insensibili (insulino-resistenza). Solitamente nel diabete di tipo 2 c’è una combinazione di entrambe le cause. In queste condizioni, si ha un accumulo di glucosio nel sangue (iperglicemia) che, a cascata, provoca una diminuzione dell’assorbimento del glucosio nei muscoli e un aumento degli acidi grassi in circolo. Questi ultimi sembrano essere collegati all’aumento della secrezione di molecole infiammatorie e al danno a molteplici organi e tessuti. Di fatto nel diabete l’infiammazione è la causa principale delle complicazioni che possono insorgere nel lungo periodo, come patologie cardiovascolari, necrosi tissutale, perdita della vista, insufficienza renale etc.
Microbiota e diabete
Quando si parla di infiammazione sistemica non si può non parlare di microbiota. Non è un caso se moltissimi studi abbiano rilevato un microbiota caratteristico della patologia diabetica. Il microbiota infatti modula l’infiammazione, interagisce con i nutrienti, influenza la permeabilità intestinale, il metabolismo del glucosio e lipidico, la sensibilità all’insulina e il bilancio energetico del corpo.
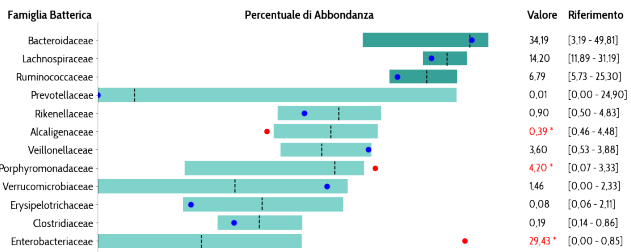
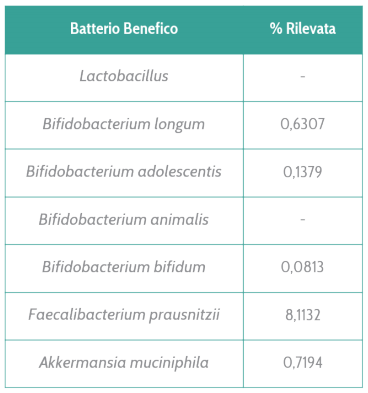
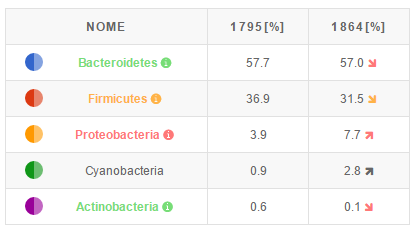
Diversi microbi intestinali possono promuovere un’infiammazione di basso grado o endotossiemia, tipica del diabete di tipo 2, e possono scalzare prepotentemente i batteri benefici. Batteri come Bifidobacterium, Bacteroides, Faecalibacterium, Akkermansia e Roseburia sono normalmente sottorappresentati nel microbiota dei diabetici mentre Ruminococcus, Fusobacterium e Blautia tendono ad aumentare. Il primo gruppo di batteri è normalmente considerato antinfiammatorio, produttore di butirrato e promotore di una bassa permeabilità intestinale. Inoltre, può avere attività inibitoria nei confronti di enzimi che degradano i carboidrati complessi, riducendo l’iperglicemia postprandiale. Al contrario, il secondo gruppo tende a favorire la produzione di molecole infiammatorie e a promuovere uno stato di alterata permeabilità intestinale.
Microbiota e farmaci
Il microbiota residente può positivamente o negativamente influenzare l’attività e l’efficacia dei farmaci utilizzati per curare il diabete. Non solo, alcuni batteri probiotici sono in sperimentazione per favorire la modifica del microbiota in senso “positivo”, per abbassare il grado di infiammazione sistemica e ristabilire il metabolismo normale del glucosio. B. lactis, B. animalis, L. plantarum, L. sakei, L. rhamnosus, sono tutti probiotici che hanno dimostrato diverse abilità nel management della patologia.
Prevenire è meglio
Ad ogni modo, sapendo che il diabete di tipo 2 è una patologia che dipende molto dalle nostre scelte, è certamente fondamentale prendere le decisioni giuste per quanto riguarda stile di vita e alimentazione. Eliminare la sedentarietà ed abbracciare uno stile di vita attivo sfavoriscono l’insulino-resistenza. Assumere alimenti ricchi di fibre e abbandonare la dieta tipicamente occidentale, che sta provocando un incremento di patologie come il diabete, sono sicuramente scelte positive per una saggia prevenzione.
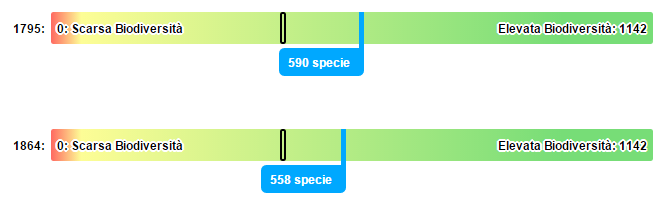
Anche monitorare il microbiota può essere uno strumento utile per verificare lo stato di disbiosi ed infiammazione sistemica. L’analisi Microbioma Italiano EVO può infatti in tal senso supportare lo specialista, anche nella definizione di una strategia nutrizionale ed integrativa ad hoc.
Alla prossima!
Eleonora Sattin, PhD
Gurung et al (2020) Role of gut microbiota in type 2 diabetes pathophysiology, The Lancet